Bilan scientifique de la dermatose nodulaire contagieuse (LSD, Lumpy Skin Disease)
- Leonard Theron
- 25 août 2025
- 7 min de lecture
Publié en première version dans Vetérinaria UPV n°3/2025
1. Introduction
La dermatose nodulaire contagieuse (Lumpy Skin Disease, LSD) est une maladie virale grave affectant principalement les bovins. La DNC est causée par un Capripoxvirus (CaPV) de la famille des Poxviridae, génétiquement proche du virus de la variole ovine et caprine. Une seule souche sérotypique est connue à ce jour. Le virus est résistant dans l’environnement et dans les croûtes cutanées séchées pendant plusieurs mois. Elle est transmise principalement par des vecteurs arthropodes, et le contact direct sur lésions.
Son expansion géographique depuis les années 2010 en Afrique, en Asie et en Europe de l’Est a soulevé des enjeux majeurs de santé animale et de sécurité économique pour les éleveurs. Elle appartient à la catégorie A des maladies règlementées en Europe (règlement UE 2016/429 : Absence du territoire, contagieuse, éradication systématique).
Figure 1 - Dermatose nodulaire contagieuse (Crédit photo Vetofocus)
2. Les symptômes
La DNC provoque :
Nodules cutanés multiples (peau, muqueuses)
Œdème, lymphadénite, fièvre forte
Baisse de production laitière, amaigrissement
Chez les veaux : formes sévères, mortalité possible
Chez les vaches laitières, une baisse de production de lait de 50 % a été rapportée pendant l’infection.

3. Morbidité et mortalité
Au cours de la dernière décennie, la morbidité associée à la LSD a été estimée entre 10 % et 85 %, selon la densité de vecteurs, la taille des troupeaux et la réponse immunitaire (Akther et al.). Les taux de mortalité au niveau national restent globalement faibles, souvent entre 1 et 5 %, bien que certains foyers mal contrôlés puissent dépasser ces chiffres, en intra-troupeau, la mortalité peut atteindre jusque 20% (Algérie, Comm. Pers.).
Dans une exploitation : atteint 50–100 % des animaux en 7 à 14 jours en l'absence de contrôle (EFSA, 2016). Entre exploitations : dépend du mouvement animal et des vecteurs – propagation régionale possible en quelques semaines à mois. Reproduction épidémique (Re) : non formellement quantifié, mais estimé entre 2 et 5 dans les zones naïves (Covid 2-5 ; FCO <2). Facteurs clés : saison des pluies, absence de vaccination, vecteurs abondants.
Les petites exploitations sont les plus vulnérables, affichant souvent des niveaux de prévalence intra-troupeau plus élevés en raison de la promiscuité animale et du manque de mesures de biosécurité (EFSA, 2017).

4. Pratiques de gestion et stratégies de contrôle
4.1 Vaccination de masse
La vaccination préventive de masse s’est imposée comme la méthode de contrôle la plus efficace. En Thaïlande, une baisse spectaculaire de l’incidence a été observée suite à l’adoption de cette stratégie (Punyapornwithaya & Arjkumpa, 2024). En Europe du Sud-Est, la vaccination d’urgence combinée à des restrictions de mouvements a permis de stopper plusieurs flambées entre 2015 et 2017 (Tuppurainen et al.).
4.2 Contrôle des mouvements et surveillance
La détection précoce, l’isolement des foyers, et la restriction des déplacements sont essentiels pour empêcher la propagation inter-troupeaux. Ces mesures ont été cruciales dans les campagnes d'éradication menées dans les Balkans (EFSA, 2018).
4.3 Lutte contre les vecteurs
Bien qu’importante, la lutte contre les insectes vecteurs (moustiques, mouches piqueuses) est souvent négligée. L’absence d’utilisation de répulsifs ou de moustiquaires dans les étables a été identifiée comme un facteur aggravant, notamment au Bangladesh (Khan et al., 2024).
4.4. Abattage des animaux positifs
L’abattage en cas de DNC constitue un levier essentiel de maîtrise sanitaire, avec deux options possibles : total ou partiel. L’abattage total permet une éradication complète du virus au sein du troupeau, réduit au maximum le risque de diffusion vers les élevages voisins, et facilite une levée plus rapide des restrictions. C’est l’approche privilégiée lorsque plusieurs cas cliniques sont présents, que la détection est tardive, ou dans les élevages à fort enjeu génétique ou reproductif. Cette mesure est jugée efficace dans les contextes où les ressources sont disponibles et des compensations sont versées aux éleveurs, comme ce fut le cas dans les Balkans (Tuppurainen et al., 2020).
Les expériences européennes passées confirment l’intérêt de l’abattage total couplé à une vaccination ciblée : c’est le seul schéma ayant permis une éradication rapide, comme en Grèce en 2015. À l’inverse, des stratégies plus modérées, comme en Bulgarie ou Turquie, ont conduit à une persistance de foyers sur 12 à 18 mois. Dans le contexte français actuel, il est recommandé de privilégier l’abattage total dans les foyers confirmés, notamment si plusieurs animaux sont atteints, tout en conservant une flexibilité pour l’abattage partiel dans les élevages indemnes de symptômes mais sous surveillance. Une communication claire et anticipée avec les éleveurs est indispensable pour garantir l’adhésion aux mesures et limiter les tensions.
Pays | Stratégie adoptée | Résultat |
Grèce (2015) | Abattage total systématique | Éradication en 6 mois |
Bulgarie | Abattage partiel + vaccination | Persistance de foyers sur 18 mois |
Turquie | Abattage limité + vaccin | Maladie endémique |
Algérie | Abattage positif, vaccination erratique | Maladie endémique |
Retour de notre confrère Algérien Dr. Radouane Zenki :
Depuis un an, croyez moi c'est la pire des maladies virales que j'ai rencontré dans ma carrière professionnelle depuis 27 ans, mis a part les mortalités, les rescapés sortent avec des séquelles dignes d'une scène de guerre: lésions cutanées, déformations des articulations déclives , stérilités et des problèmes respiratoires


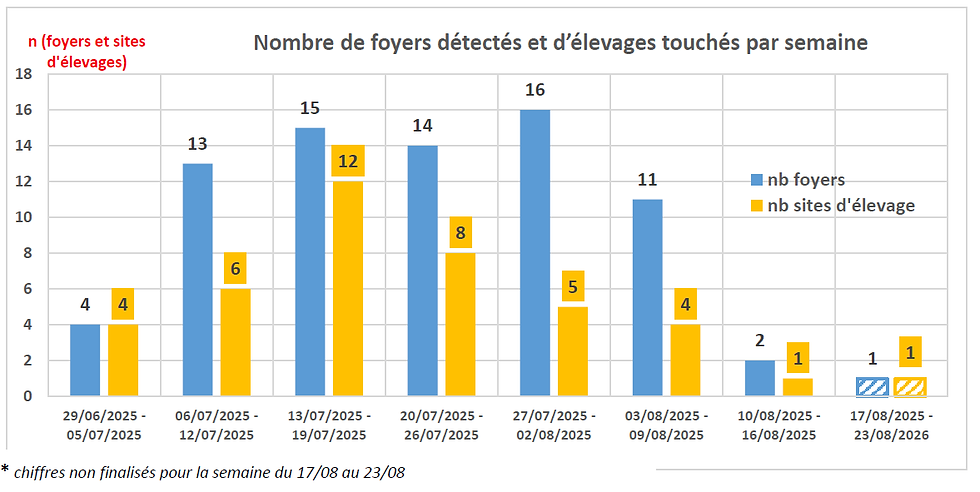
6. Foyers en France actualité
Depuis le 29 juin 2025, la Dermatose Nodulaire Contagieuse (DNC) a été confirmée dans 74 foyers bovins en France, tous localisés dans les départements de Savoie et Haute-Savoie. En réponse, les autorités françaises ont instauré la vaccination obligatoire sur un périmètre de 50 km, couvrant 310 000 bovins, avec déjà plus de 70 % des animaux vaccinés à ce jour. Les troupeaux infectés sont abattus, les mouvements d’animaux interdits, et une indemnisation rapide est mise en œuvre.
À ce stade, le risque de diffusion vers la Belgique est jugé faible, grâce à la localisation confinée des foyers, à la couverture vaccinale élevée, et à la faible capacité de déplacement des vecteurs (quelques kilomètres). Toutefois, la période de transmission vectorielle reste active jusqu’à septembre, justifiant le maintien d’une surveillance clinique renforcée, la diffusion d’outils de détection précoce, et une coordination transfrontalière. Deux scénarios sont envisagés : un optimiste avec fin de l’épidémie d’ici novembre, et un pessimiste avec foyers persistants jusqu’en hiver.
Issu du FAQ 2025 : Pourquoi ne pas éliminer uniquement les animaux qui présentent des symptômes ? Même s’ils semblent en bonne santé, les bovins d’un groupe infectés peuvent être porteurs silencieux du virus pendant plusieurs semaines. Ils peuvent contribuer à le transmettre sans qu’on puisse le détecter avec certitude, même avec des analyses de laboratoire. Ne dépeupler le foyer que de ses animaux présentant des symptômes fait prendre un risque de propagation de la maladie, car la présence du virus sera maintenue par les animaux infectés sans symptômes. De nouveaux insectes pourront être contaminés et transporter le virus vers de nouveaux groupes d’animaux. Seul le dépeuplement total du foyer permet de d’éteindre rapidement la circulation du virus. L’expérience des pays qui ont pratiqué cette méthode montre que c’est la plus efficace, associée aux autres mesures de lutte que sont le contrôle des mouvements et la vaccination. Ce fut le cas de la Bulgarie en 2016 par exemple. Précision : la stratégie de dépeuplement s’applique à un « foyer » (c’est-à-dire une unité épidémiologique), et non à un « troupeau » ou à un « élevage » (voir la question Comment compte-t-on les foyers ?).
7. Conclusions
La lutte contre la LSD a connu des succès notables dans les régions ayant mis en œuvre des stratégies intégrées : vaccination, restriction des mouvements, surveillance active et, dans certains cas, abattage stratégique. Toutefois, l’abattage systématique représente une option de plus en plus difficile en termes d’acceptation éthique. Les compensations doivent donc être importantes pour respecter la sévérité du processus de maitrise.
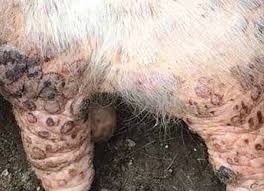
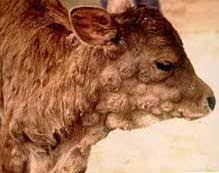
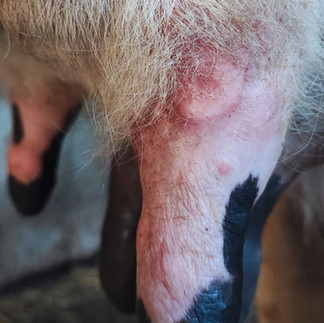
Figure 5 : lésions variées (Crédit Vetofocus(c), confrères Algériens)
Références :
EFSA Panel on Animal Health and Welfare. (2015). Scientific opinion on lumpy skin disease. EFSA Journal, 13(1), 3986. https://doi.org/10.2903/j.efsa.2015.3986
EFSA Panel on Animal Health and Welfare. (2016). Urgent advice on lumpy skin disease. EFSA Journal, 14(12), 4573. https://doi.org/10.2903/j.efsa.2016.4573
EFSA Panel on Animal Health and Welfare. (2017). Lumpy skin disease: I. Data collection and analysis. EFSA Journal, 15(3), 4773. https://doi.org/10.2903/j.efsa.2017.4773
EFSA Panel on Animal Health and Welfare. (2018). Lumpy skin disease: Scientific and technical assistance on control and surveillance activities. EFSA Journal, 16(2), 5452. https://doi.org/10.2903/j.efsa.2018.5452
EFSA Panel on Animal Health and Welfare. (2022). Assessment of the control measures for category A diseases of Animal Health Law: Lumpy Skin Disease. EFSA Journal, 20(12), 7121. https://doi.org/10.2903/j.efsa.2022.7121
Horst, H. S., De Vos, C. J., & Tomassen, F. H. M. (1999). The economic evaluation of control and eradication of epidemic livestock diseases. Bulletin of the Office International des Épizooties, 117(3), 611–620. https://www.researchgate.net/publication/12826714
Molla, W., de Jong, M. C. M., Gari, G., & Frankena, K. (2017). Economic impact of lumpy skin disease and cost effectiveness of vaccination for the control of outbreaks in Ethiopia. Preventive Veterinary Medicine, 147, 100–107. https://www.sciencedirect.com/science/article/pii/S0167587717303999
Ministère de l’Agriculture et de la Souveraineté alimentaire. (2025, août). Dermatose nodulaire contagieuse des bovins (DNC) : point de situation et foire aux questions. https://agriculture.gouv.fr/dermatose-nodulaire-contagieuse-des-bovins-dnc-point-de-situation-et-foire-aux-questions
Tuppurainen, E. S. M., Antoniou, S. E., & Tsiamadis, E. (2020). Field observations and experiences gained from the implementation of control measures against lumpy skin disease in South-East Europe between 2015 and 2017. Preventive Veterinary Medicine, 181, 105052. https://www.sciencedirect.com/science/article/pii/S0167587718305488
Tuppurainen, E., & Galon, N. (2016). Lumpy skin disease: Current situation in Europe and neighbouring regions and necessary control measures to halt the spread in south-east Europe [Technical report]. OIE. https://www.researchgate.net/publication/321937389
Lee, S., Baker, C. M., Sellens, E., & Stevenson, M. A. (2024). A systematic review of epidemiological modelling in response to lumpy skin disease outbreaks. Frontiers in Veterinary Science, 11, 1459293. https://www.frontiersin.org/journals/veterinary-science/articles/10.3389/fvets.2024.1459293/full






















Commentaires